Los geht's, Ben!
Kapitel 2.9–2.13 — interaktiv, verständlich und Schritt für Schritt erklärt.
Was dich erwartet
Chemie macht richtig Spass, sobald man die Zusammenhänge versteht. Diese Seite bringt dir Kapitel 2.9–2.13 so nah, dass du die Konzepte nicht nur auswendig kennst, sondern wirklich durchblickst. Jeder Abschnitt enthält:
- Lernziele — damit du weisst, worauf es ankommt
- Konzept — die Theorie, klar und direkt erklärt
- Formeln — mit allen Variablen und Einheiten
- Interaktive Visualisierungen — zum Ausprobieren und Begreifen
- Aufgaben — mit vollständigen Musterlösungen zum Nachschlagen
Tipp: Markiere jeden Abschnitt als «Abgeschlossen», sobald du die Aufgaben ohne Hilfe lösen kannst. Der Fortschrittsbalken oben zeigt, wie weit du schon bist — du schaffst das!
Coulomb-Energie & Coulomb-Kraft
Die elektrische Wechselwirkung zwischen Ladungen — Grundlage aller Atomchemie
Lernziele
- Die Coulomb-Energie $U$ und Coulomb-Kraft $F$ mit der richtigen Formel berechnen
- Das Vorzeichen von $U$ interpretieren (positiv = abstossend, negativ = anziehend)
- Den Einfluss von Ladungsgrösse und Abstand auf $U$ und $F$ beschreiben
- Die Einheiten korrekt verwenden (C, m, J, N)
Konzept: Was ist Coulomb-Energie?
Elektrische Wechselwirkung
Zwei Ladungen üben aufeinander eine Kraft aus — anziehend bei entgegengesetzten, abstossend bei gleichen Vorzeichen. Die Coulomb-Energie $U$ gibt an, wie viel potenzielle Energie das System der beiden Ladungen hat.
- $U < 0$: System ist stabil (Ladungen ziehen sich an) — z.B. Elektron + Proton im Atom
- $U > 0$: System ist instabil (Ladungen stossen sich ab) — z.B. zwei Protonen
- Je kleiner der Abstand $r$, desto grösser $|U|$ — die Energie «geht gegen unendlich» bei $r \to 0$
Formeln
| $U$ | Coulomb-Energie in Joule [J] |
| $k$ | Coulomb-Konstante = $8.9875 \times 10^9\ \text{N}\cdot\text{m}^2/\text{C}^2$ |
| $Q_1, Q_2$ | Ladungen in Coulomb [C] (mit Vorzeichen!) |
| $r_{12}$ | Abstand zwischen den Ladungen in Meter [m] |
| $F$ | Coulomb-Kraft in Newton [N] |
| Negatives $F$ = Anziehung, positives $F$ = Abstossung | |
| Merke: $F = dU/dr$ — Kraft ist Ableitung der Energie nach dem Abstand |
Elementarladung: $e = 1.602 \times 10^{-19}\ \text{C}$
Proton: $Q = +e = +1.602 \times 10^{-19}\ \text{C}$
Elektron: $Q = -e = -1.602 \times 10^{-19}\ \text{C}$
Interaktiv: Energie-Kurve
Ziehe den Schieberegler, um den Abstand $r$ zu verändern. Lies $U$ und $F$ live ab.
Interaktiv: Ladungsrechner
Gib eigene Werte ein und sieh die vollständige Rechnung:
Referenzbild aus dem Skript
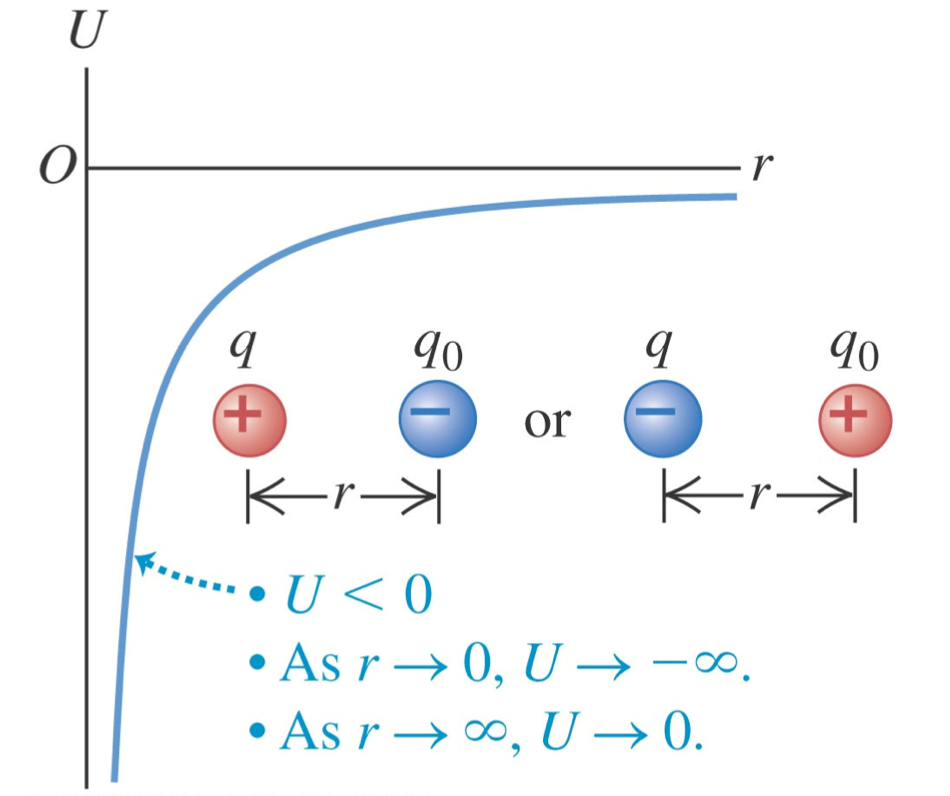
Abb. aus Skript: Coulomb-Energie als Funktion des Abstands r
Aufgaben
$U = 8.9875 \times 10^9 \cdot \frac{(+1.602 \times 10^{-19}) \cdot (-1.602 \times 10^{-19})}{53 \times 10^{-12}}$
$F = 8.9875 \times 10^9 \cdot \frac{(-2.566 \times 10^{-38})}{(53 \times 10^{-12})^2}$
Da $U \propto 1/r$ und $U \propto Q_1 \cdot Q_2$:
(a) r verdoppelt: $U$ halbiert sich ($U \to U/2$)
(b) r halbiert: $U$ verdoppelt sich ($U \to 2U$)
(c) r verdreifacht: $U$ wird ein Drittel ($U \to U/3$)
(d) Eine Ladung verdoppelt: $U$ verdoppelt sich ($U \to 2U$)
(e) Beide Ladungen verdoppelt: $U$ vervierfacht sich ($U \to 4U$)
Tipp: Der Rechner oben lässt sich nutzen, um diese Verhältnisse selbst zu prüfen.
(a) Berechne die Coulomb-Energie $U_1$ des Systems.
(b) Die Ladung $Q_2$ bewegt sich in Richtung $Q_1$, und der Abstand verringert sich auf $r_{12} = 2$. Berechne die neue Coulomb-Energie $U_2$.
(c) Berechne die Differenz $\Delta U = U_2 - U_1$.
(d) Welches System hat eine grössere Coulomb-Energie — vor oder nach der Bewegung?
(e) Wenn die freigesetzte Energie in Wärme umgewandelt würde — wäre der Prozess exotherm oder endotherm? Begründe.
Energieniveaudiagramm:
$U_1 = -0.8$ (oben, vorher) → $U_2 = -4.0$ (unten, nachher)
Pfeil nach unten: $\Delta U = -3.2$ (Energie wird als Wärme abgegeben)
Bohr-Modell & Effektive Kernladung
Wie Elektronen in Schalen angeordnet sind und was das Valenzelektron «spürt»
Lernziele
- Das Bohr-Modell beschreiben: Elektronen auf Schalen, Quantenzahlen
- Für Elemente Z=1–20 die Elektronenkonfiguration nach Schalen angeben
- Die effektive Kernladung $Z_\text{eff}$ berechnen: $Z_\text{eff} = Z - \text{Innenschalenelektronen}$
- Erklären, warum Atome in einer Periode kleiner werden (zunehmendes $Z_\text{eff}$)
Konzept: Das Bohr-Modell
Schalen und Quantenzahlen
Im Bohr-Modell bewegen sich Elektronen auf kreisförmigen Bahnen (Schalen) mit festen Energien. Jede Schale hat eine Hauptquantenzahl $n = 1, 2, 3, ...$
- Schale $n=1$: max. 2 Elektronen
- Schale $n=2$: max. 8 Elektronen
- Schale $n=3$: max. 18 Elektronen (für Z≤20 praktisch max. 8)
- Schale $n=4$: max. 32 Elektronen
Elektronen füllen von innen nach aussen auf — zuerst Schale 1, dann 2, usw.
Ernest Rutherford

Rutherford: Streuexperiment → kompakter Kern mit positivem Kern
Effektive Kernladung $Z_\text{eff}$
Das Valenzelektron «spürt» nicht die volle Kernladung $Z$, weil die inneren Elektronen abschirmen:
$$Z_\text{eff} = Z - \sigma$$wobei $\sigma$ = Anzahl Innenschalenelektronen (vereinfachtes Modell)
Beispiel Natrium (Na, Z=11):
Schalen: 2, 8, 1 → $\sigma = 10$ → $Z_\text{eff} = 11 - 10 = +1$
Beispiel Chlor (Cl, Z=17):
Schalen: 2, 8, 7 → $\sigma = 10$ → $Z_\text{eff} = 17 - 10 = +7$
Interaktiv: Atom-Builder
Effektive Ladung — Vergleich
Aufgaben
Lithium (Li, Z=3): 2, 1 (Schale 1: 2e⁻, Schale 2: 1e⁻)
Natrium (Na, Z=11): 2, 8, 1 (Schale 1: 2e⁻, Schale 2: 8e⁻, Schale 3: 1e⁻)
Chlor (Cl, Z=17): 2, 8, 7 (Schale 1: 2e⁻, Schale 2: 8e⁻, Schale 3: 7e⁻)
Kontrolle: Summe der Elektronen = Kernladung Z ✓
Li (Z=3): Schalen 2,1 → $Z_\text{eff} = 3 - 2 = +1$
F (Z=9): Schalen 2,7 → $Z_\text{eff} = 9 - 2 = +7$
Die Coulomb-Kraft ist $F \propto Z_\text{eff} / r^2$. Das Valenzelektron von F «spürt» eine 7× grössere effektive Kernladung als das von Li, bei ähnlichem Schalenradius.
→ F bindet sein Valenzelektron viel stärker → höhere Ionisierungsenergie → kleinerer Atomradius.
Ionisierungsenergie
Wie viel Energie braucht es, um ein Elektron aus einem Atom zu entfernen?
Lernziele
- Definition: Erste Ionisierungsenergie $IE_1$ = Energie, um das erste (äusserste) Elektron zu entfernen
- Den Trend der IE₁ in einer Periode erklären (steigt von links nach rechts)
- Die Ausnahmen bei B und O erklären (Beginn p-Block, halb gefülltes p-Orbital)
- Aus den sukzessiven IE erkennen, welche Elektronen zur Valenzschale gehören
Konzept: Ionisierungsenergie
Erste Ionisierungsenergie ($IE_1$)
$$\text{X}(g) \rightarrow \text{X}^+(g) + e^-$$Die Energie, die benötigt wird, um aus einem gasförmigen, neutralen Atom im Grundzustand ein Elektron zu entfernen.
- Trend Periode: IE₁ nimmt von links nach rechts zu, weil $Z_\text{eff}$ zunimmt
- Trend Gruppe: IE₁ nimmt von oben nach unten ab, weil der Radius zunimmt
- Ausnahmen: B < Be (Beginn p-Block: p-Elektronen weniger stabil als s) und O < N (halb gefülltes p-Orbital besonders stabil)
Sukzessive Ionisierungsenergien: Ein grosser Sprung zeigt, dass Kern-Elektronen erreicht wurden.
Beispiel Be: IE₁=900, IE₂=1757, IE₃=14849 kJ/mol → grosser Sprung bei IE₃ → Be hat 2 Valenzelektronen.
Interaktiv: IE₁ Grafik (Z = 1–36)
Sukzessive Ionisierungsenergien
Aufgaben
In Periode 2 nimmt die Kernladung $Z$ von 3 (Li) bis 10 (Ne) zu. Alle Valenzelektronen befinden sich auf Schale $n=2$.
Da die inneren Elektronen (Schale 1, 2e⁻) konstant bleiben, nimmt $Z_\text{eff} = Z - 2$ von +1 (Li) bis +8 (Ne) zu.
Gleichzeitig nimmt der Atomradius ab, weil das Valenzelektron stärker angezogen wird.
→ Grösseres $Z_\text{eff}$ + kleinerer Radius → stärkere Coulomb-Anziehung → höhere IE₁.
N (Z=7): Konfiguration 1s² 2s² 2p³ → alle 3 p-Orbitale einfach besetzt (Hund'sche Regel) → halb gefülltes p-Orbital ist besonders stabil.
O (Z=8): Konfiguration 1s² 2s² 2p⁴ → ein p-Orbital ist doppelt besetzt → Elektronenpaar-Abstossung → dieses Elektron lässt sich leichter entfernen.
→ IE₁(N) = 1402 kJ/mol > IE₁(O) = 1314 kJ/mol
Der grosse Sprung liegt zwischen IE₂ (1757 kJ/mol) und IE₃ (14849 kJ/mol).
→ Das 3. Elektron befindet sich bereits auf einer inneren Schale (Kernelektron) → viel schwieriger zu entfernen.
→ Be hat 2 Valenzelektronen (in Schale 2).
Bestätigung: Elektronenkonfiguration Be: 2, 2 → 2 Valenzelektronen ✓
Atome und Licht
Emissionsspektren, Flammenfarben und der Photonensprung
Lernziele
- Erklären, warum Atome diskrete Linienspektren emittieren (gequantelte Energieniveaus)
- Die Balmer-Serie des Wasserstoffs beschreiben (Übergänge $n \to 2$)
- Die Flammenfarben der Alkalimetalle kennen und erklären
- Energie, Frequenz und Wellenlänge eines Photons verknüpfen: $E = h\nu = hc/\lambda$
Konzept: Quantisierte Energieniveaus
Warum Linienspektrum?
Im Bohr-Modell können Elektronen nur auf bestimmten Energieniveaus $E_n$ existieren. Wenn ein Elektron von einem höheren Niveau $n_\text{oben}$ auf ein tieferes $n_\text{unten}$ springt, wird ein Photon mit genau der Energiedifferenz emittiert:
$$\Delta E = E_{n_\text{oben}} - E_{n_\text{unten}} = h\nu = \frac{hc}{\lambda}$$Da nur diskrete $\Delta E$ möglich sind → nur diskrete Wellenlängen → Linienspektrum.
| $h$ | Planck'sches Wirkungsquantum = $6.626 \times 10^{-34}\ \text{J}\cdot\text{s}$ |
| $\nu$ | Frequenz des Lichts in Hz [1/s] |
| $c$ | Lichtgeschwindigkeit = $3.00 \times 10^8\ \text{m/s}$ |
| $\lambda$ | Wellenlänge in Meter [m] |
Interaktiv: Emissionsspektrum Wasserstoff
Hover über eine Spektrallinie für Details. Sichtbarer Bereich: 380–700 nm.
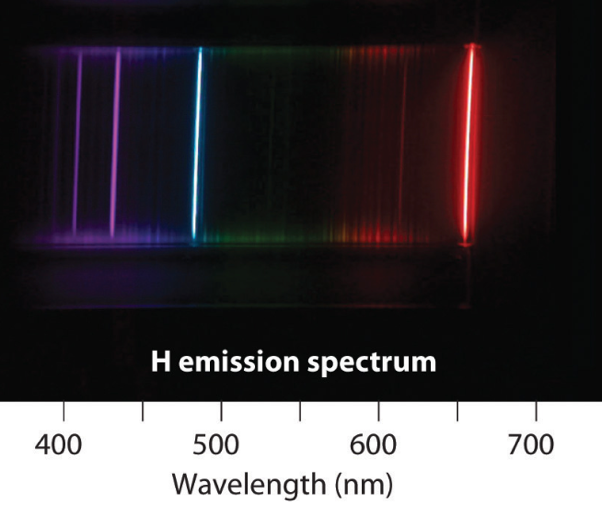
Foto: Emissionsspektrum von Wasserstoff
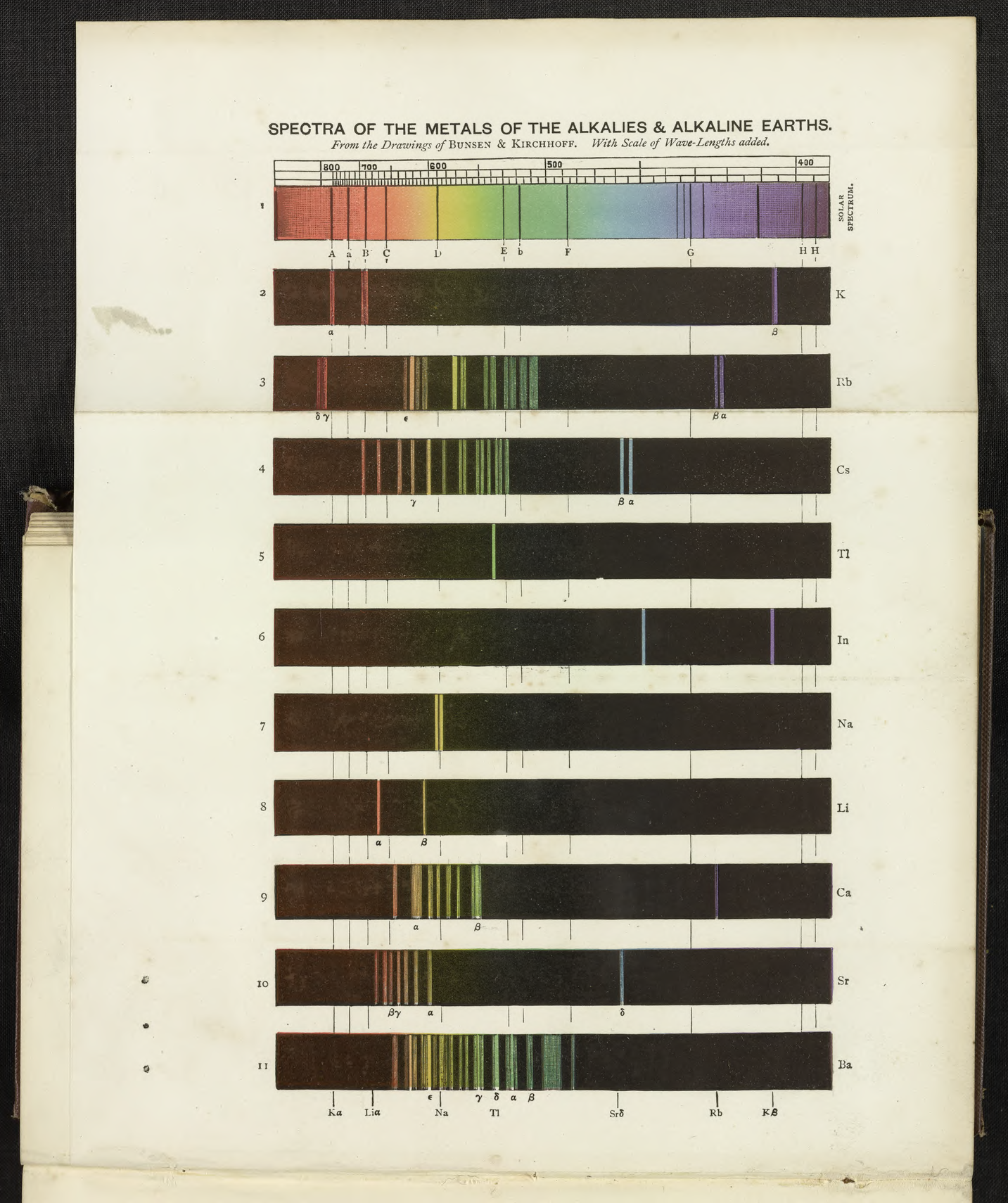
Historisches Spektrendiagramm
Energieniveau-Diagramm
Klicke auf einen Übergang, um die Wellenlänge zu sehen.
Flammenfarben
Wenn Metallsalze in eine Flamme gehalten werden, werden Elektronen angeregt und emittieren beim Zurückfallen charakteristisches Licht:
Aufgaben
Orbitale
Elektronenkonfiguration, Orbital-Kastenschema und Quantenmechanik
Lernziele
- Den Unterschied zwischen Schale (Bohr) und Orbital (Quantenmechanik) erklären
- Die Auffüllregel (Aufbau-Prinzip), Hund'sche Regel und Pauli-Prinzip anwenden
- Orbital-Kastenschemas für Z=1–20 zeichnen
- Anomalien der IE₁ mit Orbital-Besetzung erklären (N vs O, Be vs B)
Konzept: Von Schalen zu Orbitalen
Drei Grundregeln
- Aufbau-Prinzip: Orbitale werden in Reihenfolge steigender Energie besetzt: 1s → 2s → 2p → 3s → 3p → 4s → 3d → ...
- Pauli-Prinzip: Jedes Orbital fasst max. 2 Elektronen mit entgegengesetztem Spin (↑↓)
- Hund'sche Regel: Bei mehreren gleichwertigen Orbitalen (z.B. 3×2p) wird zuerst jedes einfach besetzt (↑), bevor eines doppelt besetzt wird (↑↓)
Orbitaltypen
s-Orbital: kugelförmig, 1 Orbital pro Unterschale, max. 2e⁻
p-Orbital: hantelförmig, 3 Orbitale (x,y,z), max. 6e⁻
d-Orbital: komplex, 5 Orbitale, max. 10e⁻
Auffüllreihenfolge merken: 1s 2s 2p 3s 3p 4s 3d 4p ...
In jedem Orbital befinden sich IMMER max. 2 Elektronen mit entgegengesetztem Spin.
- Ein halbgefülltes Orbital (ein Elektron, ↑) ist besonders stabil → erklärt erhöhte IE₁ bei N, Cr, Mo
- Ein vollgefülltes Orbital (↑↓) hat erhöhte Abstosskraft → erklärt erniedrigte IE₁ bei O

Orbital-Energieniveaus aus dem Skript
Interaktiv: Orbital-Kastenschema
IE-Anomalien erklärt
Warum BE > B bei IE₁?
Be: 1s² 2s² — beide Valenzelektronen im s-Orbital (stabiler als p)
B: 1s² 2s² 2p¹ — das p-Elektron ist energetisch höher und leichter zu entfernen → IE₁(B) < IE₁(Be)
Allgemein: Beim Wechsel vom s- zum p-Block sinkt die IE₁ leicht.
Aufgaben
Stickstoff N (Z=7): 1s² 2s² 2p³
1s: [↑↓] | 2s: [↑↓] | 2p: [↑][↑][↑]
→ Hund'sche Regel: jedes 2p-Orbital einfach besetzt. Halb gefülltes p → besonders stabil.
Neon Ne (Z=10): 1s² 2s² 2p⁶
1s: [↑↓] | 2s: [↑↓] | 2p: [↑↓][↑↓][↑↓]
→ Alle Orbitale vollständig besetzt → Edelgaskonfiguration, sehr stabil.
P (Z=15): 1s² 2s² 2p⁶ 3s² 3p³ → 3p: [↑][↑][↑] (halbgefüllt, stabil)
S (Z=16): 1s² 2s² 2p⁶ 3s² 3p⁴ → 3p: [↑↓][↑][↑] (ein Orbital doppelt besetzt)
Das doppelt besetzte 3p-Orbital von S hat erhöhte Elektronen-Elektronen-Abstossung → dieses Elektron ist leichter zu entfernen → IE₁(S) < IE₁(P).
IE₁(P) = 1011 kJ/mol, IE₁(S) = 1000 kJ/mol — der Unterschied ist klein aber messbar.
Das 4s-Orbital hat bei neutralen Atomen eine tiefere Energie als das 3d-Orbital (die Energie hängt von der Abschirmung durch andere Elektronen ab).
→ Aufbau-Prinzip: Orbitale werden in Reihenfolge steigender Energie besetzt: ... 3p → 4s → 3d → 4p ...
Kalium K (Z=19): Konfiguration = [Ar] 4s¹
Das 19. Elektron geht ins 4s-Orbital, nicht ins 3d!
→ K ist ein Alkalimetall (s-Block) mit einem Valenzelektron.
Atom-Poster Builder
Erstelle ein vollständiges Atom-Steckbriefposter für jedes Element
Wähle ein Element — das Poster wird automatisch generiert mit Bohr-Modell, Elektronenkonfiguration, Ionisierungsenergie und mehr.
Zusammenfassung & Selbsttest
Hake ab, was du beherrschst — und feiere jeden Haken!
Lernziele-Checkliste
Wichtige Formeln
Alle Formeln auf einen Blick
$$U = k \cdot \frac{Q_1 \cdot Q_2}{r} \qquad F = k \cdot \frac{Q_1 \cdot Q_2}{r^2}$$
$$Z_\text{eff} = Z - \sigma \qquad E_\text{Photon} = \frac{hc}{\lambda}$$
$k = 8.9875 \times 10^9\ \text{N}\cdot\text{m}^2/\text{C}^2$ | $e = 1.602 \times 10^{-19}\ \text{C}$ | $h = 6.626 \times 10^{-34}\ \text{J}\cdot\text{s}$ | $c = 3.00 \times 10^8\ \text{m/s}$
Selbsttest (5 Fragen)
$k = 8.9875 \times 10^9\ \text{N}\cdot\text{m}^2/\text{C}^2$ | $e = 1.602 \times 10^{-19}\ \text{C}$ | $h = 6.626 \times 10^{-34}\ \text{J}\cdot\text{s}$ | $c = 3.00 \times 10^8\ \text{m/s}$